Sólido, líquido e gasoso, são três estados físicos das substâncias químicas, que podem sofrer mudanças entre elas. Em um dia mais quente, por exemplo, ao tirarmos um gelo do congelador, podemos perceber que começa a derreter, passando, então, do estado sólido para o estado líquido. Temos alguns tipos de passagem: do sólido para o líquido, chamamos de fusão; do líquido para o gasoso, chamamos de vaporização; de gasoso para sólido, condensação; do líquido para o sólido, solidificação; e, por fim, a mudança entre os estados sólido e gasoso são chamadas de sublimação.
Publicidade

Como se dá a solidificação
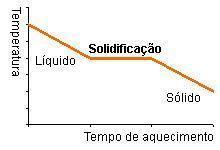
Neste artigo, vamos tratar da solidificação que é, portanto, a mudança do estado líquido para o sólido, como a reação inversa da que mencionamos anteriormente falando sobre o gelo: a água virando gelo. A passagem do estado líquido para o sólido se dá por meio do resfriamento ou arrefecimento, porém quando a substância, antes líquida, começa a solidificar, ela mantém a temperatura até que esteja completamente sólida para, posteriormente, continuar a diminuir sua temperatura, conforme demonstrado no gráfico abaixo. A água, por exemplo, tem como ponto de solidificação a temperatura de 0°C, permanecendo líquida até esse ponto e, passando disso, permanecerá nos 0° até que se torne totalmente sólida, caindo, posteriormente, para -1°C ou -2°C, e assim por diante.
Trata-se, portanto, da transformação física exotérmica de uma substância que, ao perder calor, tem suas forças repulsivas intermoleculares do estado sólido diminuídas até que se tornem próximas às forças atrativas. Com isso, o grau de agitaçãodas moléculas diminui, diminuindo também a energia do poço de potencial, não mais permitindo o escoamento das partículas.
Nesse ponto, surgem os “germes de nucleação”, que são pequenos cristais que se formam e em torno dos quais as outras partículas começarão a se agregar, unindo-se e compactando-as. Depois disso, variando de acordo com a substância pura ou mistura eutética, a temperatura ficará constante, de forma que o estado sólido acabará se formando. Nesse processo, a energia extraída passa a aumentar a energia potencial, sem diminuir a energia cinética. Quando se trata de outro tipo de mistura, entretanto, a energia se distribuirá entre as funções de diminuir a energia cinética e aumentar a energia potencial.
A solidificação somente acontecerá quando a energia extraída do sistema for o suficiente para que supra a variação positiva da energia potencial, ou ainda nas substâncias com constante fusão, a variação negativa da energia cinética deve ser capaz de trazer o fortalecimento da atração eletrostatica entre si, permitindo que haja um raio médio pequeno quando comparado às fimensões das partículas. Essa seria a propriedade da solidez.
Termodinâmica da solidificação
Segundo o conceito introduzido por Joseph Black (1728 – 1799), a energia perdida no processo deve ser igual ao calor desolidificação. O calor liberado durante a troca de fases irá depender da massa da substância que será solidificada, assim como do calor latente, que é variável de acordo com cada substância e suas propriedades específicas.
Q = mL onde Q representa o calor liberado, m a massa e L o calor latente de solidificação. O calor é medido em Joules, enquanto a massa em quilogramas e o calor latente é em joules por quilograma. Quando se trata de substância pura ou mistura eutética, a temperatura permanecerá constante durante o período de mudança de fase. Isso pode ser usado, inclusive para encontrar o grau de pureza da substância.
Publicidade
Referências
Solidificação: fundamentos e aplicações – A Garcia
http://www.if.ufrgs.br/cref/amees/conden.html

Por Natália Petrin
Formada em Publicidade e Propaganda. Atualmente advogada com pós-graduação em Lei Geral de Proteção de Dados e Direito Processual Penal. Mestranda em Criminologia.
Petrin, Natália. Solidificação. Todo Estudo. Disponível em: https://www.todoestudo.com.br/quimica/solidificacao. Acesso em: 03 de December de 2024.
01. [Facimpa – MG] Observe:
I – Uma pedra de naftalina deixada no armário;
II – Uma vasilha de água deixada no freezer;
III- Uma vasilha de água deixada no fogo;
IV – O derretimento de um pedaço de chumbo quando aquecido;
Nesses fatos estão relacionados corretamente os seguintes fenômenos:
a) I. Sublimação; II. Solidificação; III. Evaporação; IV. Fusão.
b) I. Sublimação; II. Sublimação; III. Evaporação; IV. Solidificação.
c) I. Fusão; II. Sublimação; III. Evaporação; IV. Solidificação.
d) I. Evaporação; II. Solidificação; III. Fusão; IV. Sublimação.
e) I. Evaporação; II. Sublimação; III. Fusão; IV. Solidificação.
02. [UFPR] A água pode ser encontrada na natureza nos estados sólido, líquido ou gasoso. Conforme as condições, a água pode passar de um estado para outro através de processos que recebem nomes específicos. Um desses casos é quando ela muda do estado gasoso para o líquido.
Assinale a alternativa que apresenta o nome correto dessa transformação.
a) Sublimação.
b) Vaporização.
c) Solidificação.
d) Condensação.
e) Fusão.
01. [A]
02. [D]